
一、简 介
西安大兴医院药物(器械)临床试验伦理委员会(以下简称伦理委员会)成立于2019年,对我院实施的药物/器械临床研究进行伦理审查。目前伦理委员会设有主任委员1名、副主任委员1名,委员8名;伦理委员会办公室主任1名,秘书1名。委员组成包括医学、伦理学、法学等不同学科的专家及社区代表。伦理委员会办公室位于陕西省西安市莲湖区大兴东路33号西安大兴医院东院区,负责伦理委员会日常工作。
二、宗 旨
本伦理委员会的宗旨是通过对临床研究项目的科学性、伦理合理性进行审查,保护参加临床试验的受试者的尊严、安全和权益,促进生物医学研究达到科学和伦理的高标准,增强公众对临床研究的信任和支持。
三、工作原则
本伦理委员会以世界医学会《赫尔辛基宣言》为原则,以维护人类的健康权益、促进医学科学的发展为工作目标,遵循“尊重、不伤害、有益、公正”这四项生命伦理基本原则,高质量地开展有效的伦理审查和促进医学临床伦理建设。本医学伦理委员会在遵守国家法律、法规和有关文件的前提下独立开展伦理审查工作和活动,不受任何参与试验的申办者、研究者的影响,并接受卫生行政管理部门、药品监督管理部门的指导和监督。伦理委员会和知情同意书是保障受试者的主要措施。
四、工作职责
1、伦理委员会对本单位承担和/或实施的涉及人的生物医学研究项目进行独立、称职和及时的审查。审查范围包括药物临床试验项目,医疗器械临床试验项目,涉及人的临床科研项目(包括临床流行病学研究,利用人的医疗记录和个人信息的研究,利用人的生物标本的研究)等。
2、对已批准的临床研究进行跟踪审查,审查研究进展期间出现的严重不良事件,暂停或终止已批准的临床研究。
3、通过为研究者和医学专业人员开展继续教育,向研究者和医学专业人员提供生物医学研究和医学临床中的伦理问题的咨询和指导。
4、遵循保密原则,对伦理审查的相关资料和信息进行保密,包括受试者基本信息、研究资料信息及其他需要保密的信息。
5、伦理委员会每月召开一次会议,也可根据需要增加会议次数。
6、伦理委员会成员应接受有关医学伦理学和卫生法律法规、标准操作规程等的继续教育和培训,不断提升委员的素质和审查能力。
7、伦理委员会设置办公室,负责伦理委员会日常事务工作。
五、工作程序
1、伦理委员会秘书负责接收申请者的有关资料,包括伦理审查申请表、试验方案、病例报告表、受试者知情同意书、国家药品监督管理局的临床批件复印件(加盖红章)等。
2、伦理委员会秘书对申请者的资料进行初步审查,符合送审要求者,上报伦理委员会主任委员。
3、伦理委员会主任委员决定开会时间(受理申请一个月内)。原则上每月下旬召开会议(特殊情况除外)。
4、伦理委员会秘书在开会前三天将开会时间和地点通知各位委员,并将试验方案等资料送至委员,也可通过邮件送审。
5、伦理委员会会议每次会议参会委员人数不应少于总人数的半数,且不得少于5人。秘书作会议记录。对申报的研究项目的审查意见应在充分讨论后,以投票方式做出决定。必要时,可邀请独立顾问出席会议,就临床研究项目的某方面问题提供咨询意见,但独立顾问不参加投票。
6、秘书根据会议意见起草伦理审查批件,主任委员签发书面意见。伦理委员会的意见可以是:Ⅰ.同意;Ⅱ.作必要修改后同意;Ⅲ.作必要修改后重审;Ⅳ.不同意;Ⅴ.暂停或终止已批准的试验。
7、伦理审审查批件经主任委员签字并加盖伦理委员会公章后生效。申报审核资料及相关记录应保存至试验结束后5年。
六、人员组成(2020年版)
西安大兴医院药物(器械)临床试验伦理委员会人员组成(人体生物医学研究)
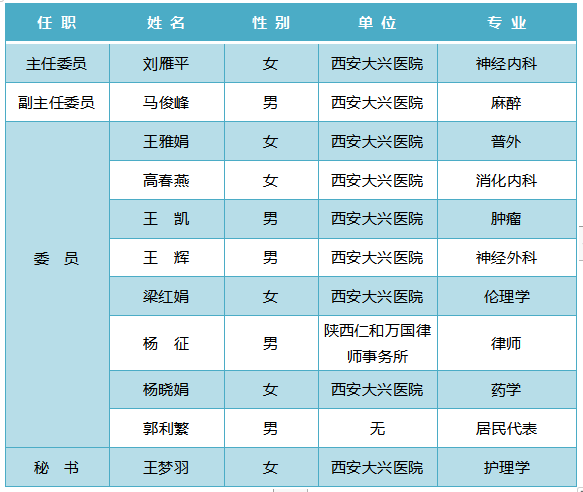
本伦理委员会的职责、人员构成、运行、记录均遵循《药物临床试验质量管理规范》(GCP)、ICH-GCP及《涉及人的生物医学研究伦理审查办法(2016)》等相关法规。